วัคซีนที่รัฐบาลไทยนำเข้ามานั้นล้วนเป็นวัคซีนที่ต่างประเทศผลิตขึ้นมาทั้งสิ้น อาทิ วัคซีนตัวเต็งที่ฉีดให้แก่ประชาชนเป็นหลัก อย่างซิโนแวค (Sinovac) ซึ่งเป็นวัคซีนสัญชาติจีน และ แอสตราเซเนกา (AstraZeneca) วัคซีนจากบริษัทสัญชาติสวีเดน-อังกฤษ ที่แม้จะเลือกบริษัท สยามไบโอไซเอนซ์ ให้ผลิตในไทย แต่ก็ไม่ถือเป็นวัคซีนที่มีกระบวนการคิดค้นและวิจัยโดยคนไทย หรือกล่าวได้ว่า ไม่ใช่วัคซีนสัญชาติไทยนั่นเอง
อย่างไรก็ตาม ขณะนี้ไทยเองก็ได้มีการผลิตวัคซีนสัญชาติไทยขึ้นมาอยู่ไม่น้อย โดยมีบุคลากรทางการแพทย์และนักวิจัยของไทยเองที่เป็นผู้คิดค้นและทำการวิจัย ซึ่งวัคซีนส่วนใหญ่ผ่านขั้นตอนการทดลองในสัตว์อย่างลิงและหนูมาแล้ว และมีผลลัพธ์ที่ดี จนถึงขณะนี้อยู่ในขั้นตอนการทดสอบกับมนุษย์
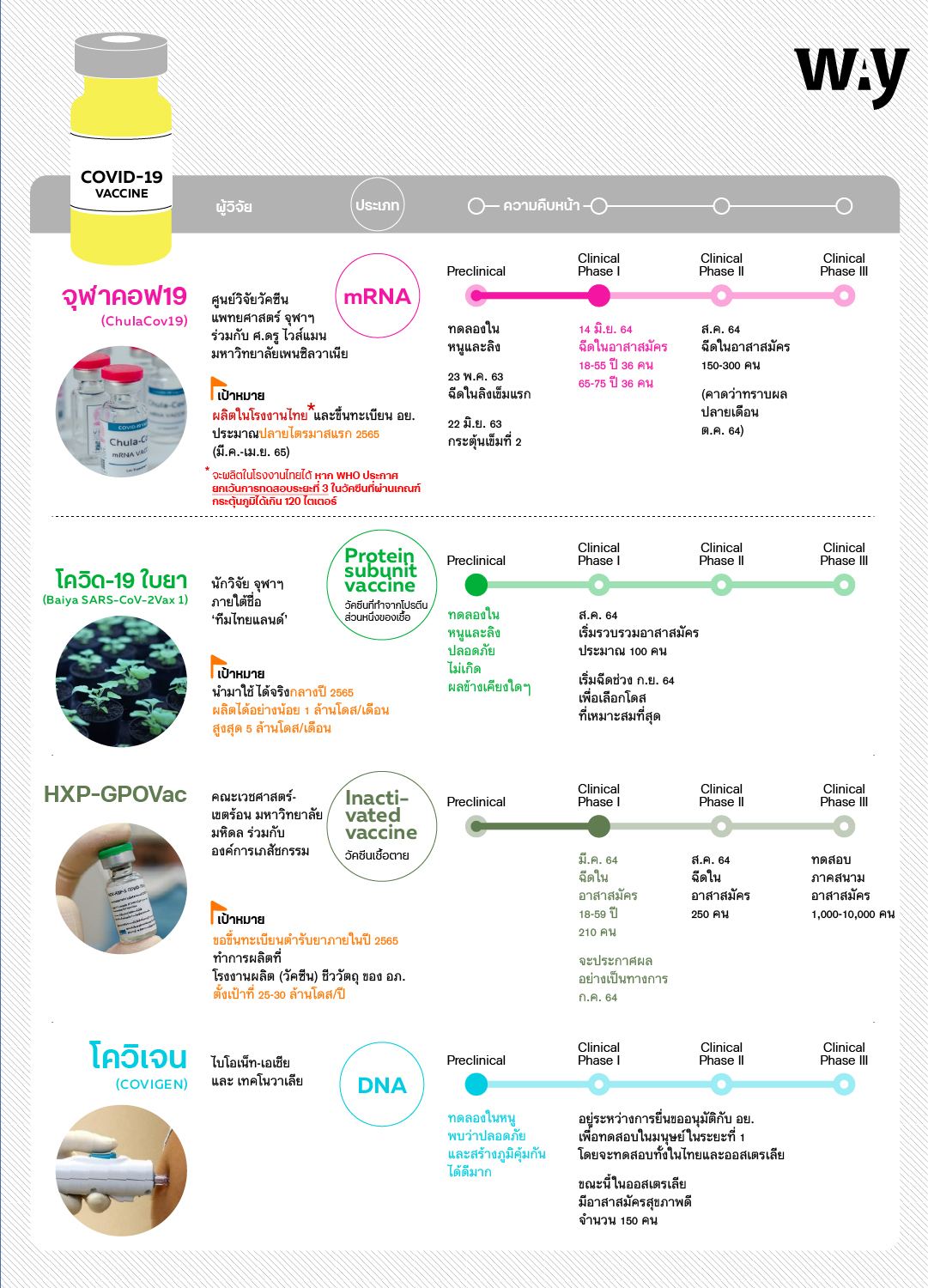
WAY รวบรวมวัคซีนจากฝีมือนักวิจัยไทยที่ขณะนี้มีทั้งหมด 4 ยี่ห้อ เพื่อให้ทุกคนได้ทำความรู้จักกับวัคซีนเหล่านี้ ว่าใครหรือหน่วยงานใดเป็นผู้คิดค้น ทำการวิจัย และผลิต ทั้งดูว่าแต่ละตัวอยู่ในขั้นตอนไหนบ้าง และคาดว่าจะสามารถนำมาให้คนไทยได้ฉีดกันในอีกไม่นานนี้อย่างแน่นอน
จุฬาคอฟ19 (ChulaCov19)
‘ChulaCov19’ หรือ ‘จุฬาคอฟ19’ เป็นวัคซีนที่ศูนย์วิจัยวัคซีน คณะแพทยศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย ร่วมมือกับหมอนักวิทยาศาสตร์ ศาสตราจารย์ดรู ไวส์แมน (Prof. Drew Weissman) แห่งมหาวิทยาลัยเพนซิลวาเนีย เพื่อพัฒนาวัคซีนป้องกันโรคโควิด-19 ชนิด mRNA โดยได้รับการสนับสนุนทุนจากสำนักงานการวิจัยแห่งชาติ (วช.) ที่มอบให้สถาบันวัคซีนแห่งชาติ และศูนย์วิจัยวัคซีน คณะแพทยศาสตร์ จุฬาฯ รวมถึงการสนับสนุนจากกองทุนศตวรรษที่ 2 จุฬาลงกรณ์มหาวิทยาลัย และเงินบริจาคจากสมาคมศิษย์เก่าแพทย์จุฬาฯ กองทุนบริจาควิจัยวัคซีน สภากาชาดไทย
วัคซีนตัวนี้เป็นวัคซีนชนิดเดียวกับไฟเซอร์ (Pfizer) และโมเดอร์นา (Moderna) ที่นำชิ้นส่วนสารพันธุกรรมของเชื้อโควิด-19 (mRNA) ส่วนที่เกี่ยวข้องกับการสร้างโปรตีนที่เป็นปุ่มหนามของเชื้อไวรัส (Spike Protein) มาสังเคราะห์เป็นรหัสคำสั่งที่เรียกว่า S-spike mRNA เมื่อฉีดวัคซีนชนิด mRNA เข้าสู่ร่างกาย จะทำให้เซลล์ในร่างกายผลิตโปรตีนส่วนที่เป็นปุ่มหนามของไวรัสขึ้น และโปรตีนที่ผลิตในส่วนนี้จะทำหน้าที่เป็นตัวกระตุ้นภูมิคุ้มกัน (antigen) ให้ร่างกายรู้จักกับเชื้อไวรัสโควิด-19 และสร้างภูมิคุ้มกัน (antibody) เพื่อป้องกันการเจ็บป่วยหรือเสียชีวิตจากโรคโควิด-19
วัคซีน ChulaCov19 มีการทดลองในหนูและลิง โดยจากการทดลองในหนู พบว่าเลือดหนูมีระดับแอนติบอดีที่สามารถยับยั้งเชื้อในหลอดทดลองได้เมื่อมีการเจือจางไปแล้ว 100 เท่า ต่อมาอีก 1 เดือน ได้ทดลองฉีดวัคซีนเข็มที่ 2 หลังจากนั้น 2 สัปดาห์ ได้ตรวจวัดระดับแอนติบอดีในเลือดอีกครั้ง พบว่ามีระดับแอนติบอดีที่สามารถยับยั้งเชื้อในหลอดทดลองได้เมื่อมีการเจือจางเลือดไปแล้วถึง 40,000 เท่า ซึ่งถือว่าอยู่ในเกณฑ์ที่สูงมาก และยังสามารถลดจำนวนเชื้อได้สูงในหนูทดลองอีกด้วย
นอกจากการทดลองในหนูแล้ว ยังมีการทดลองในลิงด้วย โดยเริ่มฉีดเข็มแรกเมื่อวันที่ 23 พฤษภาคม 2563 และฉีดวัคซีนกระตุ้นเข็มที่ 2 เมื่อวันที่ 22 มิถุนายน 2563 พบว่า สามารถกระตุ้นภูมิคุ้มกันในลิงได้ในระดับสูงมาก โดยมีระดับแอนติบอดียับยั้งเชื้อได้เมื่อเจือจางถึง 5,000 เท่า
จากผลการทดลองต่างๆ ข้างต้น พบว่าวัคซีนตัวนี้สามารถช่วยยับยั้งไม่ให้เชื้อไวรัสเข้าสู่กระแสเลือด และสามารถสร้างภูมิคุ้มกันในระดับสูงได้ จึงนำมาสู่การผลิต และทดสอบทางคลินิกระยะที่ 1 ให้กับอาสาสมัคร เมื่อวันที่ 14 มิถุนายน 2564 เป็นวันแรก ภายใต้การควบคุมดูแลจากหลายภาคส่วน รวมถึงทีมแพทย์ผู้เชี่ยวชาญของศูนย์วิจัยวัคซีน คณะแพทยศาสตร์ จุฬาฯ
การทดสอบครั้งนี้แบ่งเป็น 2 กลุ่มอายุ กลุ่มแรก เป็นอาสาสมัครอายุ 18-55 ปี จำนวน 36 คน กลุ่มที่สอง เป็นอาสาสมัครอายุ 65-75 ปี จำนวน 36 คน รวมทั้งสิ้น 72 คน
ทั้งสองกลุ่มยังถูกแบ่งเป็นกลุ่มย่อย สำหรับการฉีดวัคซีน 10, 25 และ 50 ไมโครกรัม เพื่อดูว่าวัคซีน ChulaCov19 มีประสิทธิภาพสูงสุดที่ปริมาณเท่าไร เมื่อเทียบกับวัคซีนโมเดอร์นาที่ต้องใช้ในปริมาณ 100 ไมโครกรัม และไฟเซอร์ 30 ไมโครกรัม
ทางศูนย์วิจัยวัคซีน คณะแพทยศาสตร์ จุฬาฯ จึงต้องศึกษาว่าคนไทยหรือคนเอเชียนั้นเหมาะกับการฉีดในปริมาณ 10, 25 หรือ 50 ไมโครกรัม เพื่อให้ทราบถึงขนาดที่ปลอดภัยและกระตุ้นภูมิได้สูง โดยผลทดสอบในคนระยะแรกจะรู้ผลปลายเดือน กรกฎาคม 2564 ก่อนเข้าสู่การทดสอบทางคลินิกระยะที่ 2
การทดสอบในระยะที่ 2 จะรับอาสาสมัครจำนวน 150-300 คน โดยคาดว่าจะเริ่มต้นฉีดได้ประมาณเดือนสิงหาคม และคาดว่าจะทราบผลในปลายเดือนตุลาคมนี้
อย่างไรก็ตาม การผลิตวัคซีนต้องมีการทดสอบ 3 ระยะ ตามมาตรฐานสากล และต้องฉีดในคนอีกประมาณ 15,000-30,000 คน เพื่อจะดูว่าวัคซีนสามารถป้องกันโรค ป้องกันการเกิดอาการรุนแรง และป้องกันไม่ให้เสียชีวิตได้จริงหรือไม่
นอกจากนี้ ศูนย์วิจัยวัคซีน คณะแพทยศาสตร์ จุฬาฯ ได้ทำการเตรียมความพร้อมพัฒนาวัคซีนรุ่นที่ 2 กับสัตว์ทดลองควบคู่กันไปกับรุ่นแรก เพื่อรองรับเชื้อดื้อยาหรือเชื้อกลายพันธุ์ เช่น สายพันธุ์อังกฤษ สายพันธุ์อินเดีย สายพันธุ์แอฟริกาใต้ สายพันธุ์บราซิล ฯลฯ หากทุกอย่างเป็นไปตามแผน คาดว่าจะสามารถผลิตวัคซีนที่ใช้ป้องกันเชื้อกลายพันธุ์และดื้อวัคซีนได้ เพื่อทดสอบในอาสาสมัครภายในไตรมาส 4 ของปีนี้
ทั้งนี้ เมื่อวันที่ 24 มิถุนายน 2564 สำนักข่าวบีบีซีไทย ได้รายงานคำให้สัมภาษณ์ของ ศ. นพ.เกียรติ รักษ์รุ่งธรรม ผู้อำนวยการบริหารโครงการพัฒนาวัคซีนโควิด-19 ศูนย์วิจัยวัคซีน คณะแพทยศาสตร์ จุฬาฯ ที่กล่าวไว้ว่า “ถ้าก่อนปลายปีนี้องค์การอนามัยโลก (WHO) สรุปออกมาได้ว่า ไตเตอร์หรือภูมิในน้ำเหลือง แอนติบอดี ต้องการแค่ 120 ไตเตอร์ วัคซีนไหนผ่านเกณฑ์ กระตุ้นภูมิได้เกิน 120 ไตเตอร์ ก็ไม่ต้องทำการทดสอบระยะที่ 3 ถ้าเป็นอย่างนั้นเราน่าจะมีวัคซีนที่ผลิตในโรงงานไทยแล้วขึ้นทะเบียนต่อสำนักงานคณะกรรมการอาหารและยา (อย.) ได้ภายในปลายไตรมาสที่ 1 ของปีหน้า ก็คือประมาณเดือนมีนาคม-เมษายน 2565”
โควิด-19 ใบยา

วัคซีน ‘โควิด-19 ใบยา’ ถูกพัฒนาโดยทีมนักวิจัยจุฬาฯ ภายใต้ชื่อทีมไทยแลนด์
และจากการรายงานของสำนักข่าว PPTV Online ในวันที่ 24 มิถุนายน 2564 รายงานว่า ผศ.ภญ.ดร.สุธีรา เตชคุณวุฒิ อาจารย์ประจำคณะเภสัชศาสตร์ จุฬาฯ และประธานกรรมการ บริษัท ใบยา ไฟโตฟาร์ม จำกัด หนึ่งในทีมพัฒนาวัคซีนโควิด-19 จากใบยาหรือใบพืช กล่าวถึงความคืบหน้าล่าสุดว่า วัคซีนตัวดังกล่าวกำลังเข้าสู่ขั้นตอนการศึกษาในมนุษย์ โดยได้ผ่านการทดลองในสัตว์ทดลอง คือหนูขาวและลิง ด้วยการฉีด 2 เข็ม ห่างกัน 3 สัปดาห์ และผลการทดสอบปรากฏว่าลิงมีความปลอดภัย และไม่เกิดผลข้างเคียงใดๆ ผลเลือดในลิงที่ใช้ทดลองมีค่าเอนไซม์ตับปกติ เช่นเดียวกับจำนวนเม็ดเลือดแดงและเม็ดเลือดขาว นอกจากนี้เมื่อนำเปปไทด์ไปกระตุ้นเซลล์ของลิง พบว่า มีการกระตุ้น T Cell (เซลล์ที่เจริญเติบโตแถวต่อมไธมัสบริเวณลำคอ ซึ่งเซลล์ตัวนี้ถือเป็นหัวใจหลักในการปรับระบบภูมิคุ้มกันของร่างกายให้ตอบสนองกับเชื้อโรค) ได้ดี จึงนับว่าการทดลองดังกล่าวประสบผลสำเร็จและเป็นที่น่าพอใจ
วัคซีนใบยา เป็นวัคซีนทางเลือกป้องกันโควิด-19 ที่ผลิตจากใบยาสูบสายพันธุ์ที่มีนิโคตินระดับน้อยมาก และเป็นการนำเทคนิคการใช้พืชเพื่อผลิตโปรตีน เพื่อใช้เป็นยาโมโนโคลนอลแอนติบอดี (monoclonal antibody หรือ โปรตีนที่สามารถเป็นชีววัตถุเพื่อการรักษาโรคได้) เป็นเทคโนโลยีที่มีมากว่า 15 ปีแล้ว และเคยทำสำเร็จในการรักษาโรคอีโบลามาก่อน โดยปัจจุบันโรงงานอุตสาหกรรมยาหลายแห่งทั่วโลกใช้โปรตีนจากพืชเพื่อผลิตเป็นยาหรือวัคซีน เช่น สหรัฐอเมริกา แคนาดา เยอรมนี เกาหลี ญี่ปุ่น เป็นต้น
อย่างไรก็ตาม วัคซีนโควิด-19 ใบยา เทียบเท่าได้กับวัคซีนโนวาแวกซ์ (Novavax) ของสหรัฐอเมริกา ซึ่ง ผศ.ภญ.ดร.สุธีรา กล่าวว่า หากเทียบเทคโนโลยีการผลิต วัคซีนโนวาแวกซ์จะใช้เซลล์แมลงในการผลิต ส่วนวัคซีนโควิด-19 ใบยา จะใช้ต้นไม้หรือพืช ซึ่งการวิจัยและพัฒนาครั้งนี้ ส่วนหนึ่งมาจากการระดมทุนผ่านการบริจาคของประชาชนคนไทย คนละ 500 บาท โดยมูลนิธิซียูเอ็นเทอร์ไพรส์ ผ่านโครงการวัคซีนเพื่อคนไทย โดยทีมวิจัย บริษัท ใบยา ไฟโตฟาร์ม จำกัด มีข้อตกลงกับมูลนิธิฯ ให้กำหนดราคาวัคซีนให้คนไทยในราคาต้นทุน เบื้องต้นคาดว่าจะอยู่ที่ไม่เกิน 300-500 บาทต่อโดส
การผลิตวัคชีนจากใบยาสูบนี้สามารถผลิตได้ประมาณ 10,000 โดสต่อเดือน ในห้องทดลองขนาดเล็ก จึงนับเป็นอีกหนึ่งทางเลือกที่มีประสิทธิภาพในการป้องกันโรคระบาดในอนาคต
ในเดือนสิงหาคม 2564 จะเริ่มรวบรวมอาสาสมัครประมาณ 100 คน อายุ 18-55 ปี และ 65-75 ปี และจะเริ่มฉีดช่วงเดือนกันยายน โดยการฉีดวัคซีนจะแบ่งเป็น 3 โดส ต่ำ กลาง สูง เพื่อเลือกโดสที่เหมาะสมที่สุด และดูว่าวัคซีนปริมาณขนาดใดที่สามารถนำมาใช้ในมนุษย์ได้ หากผลิตวัคซีนแล้วเสร็จ ประชาชนสามารถมากระตุ้นภูมิ โดยฉีดวัคซีนใบยาเป็นเข็มที่ 3 ได้
เบื้องต้น ผศ.ภญ.ดร.สุธีรา เตชคุณวุฒิ ตั้งเป้าไว้ว่าหากการทดสอบสำเร็จ จะสามารถผลิตวัคซีนได้อย่างน้อย 1 ล้านโดสต่อเดือน หรือสูงสุด 5 ล้านโดสต่อเดือน และคาดว่ากลางปี 2565 จะสามารถนำมาใช้ได้จริง
HXP-GPOVac
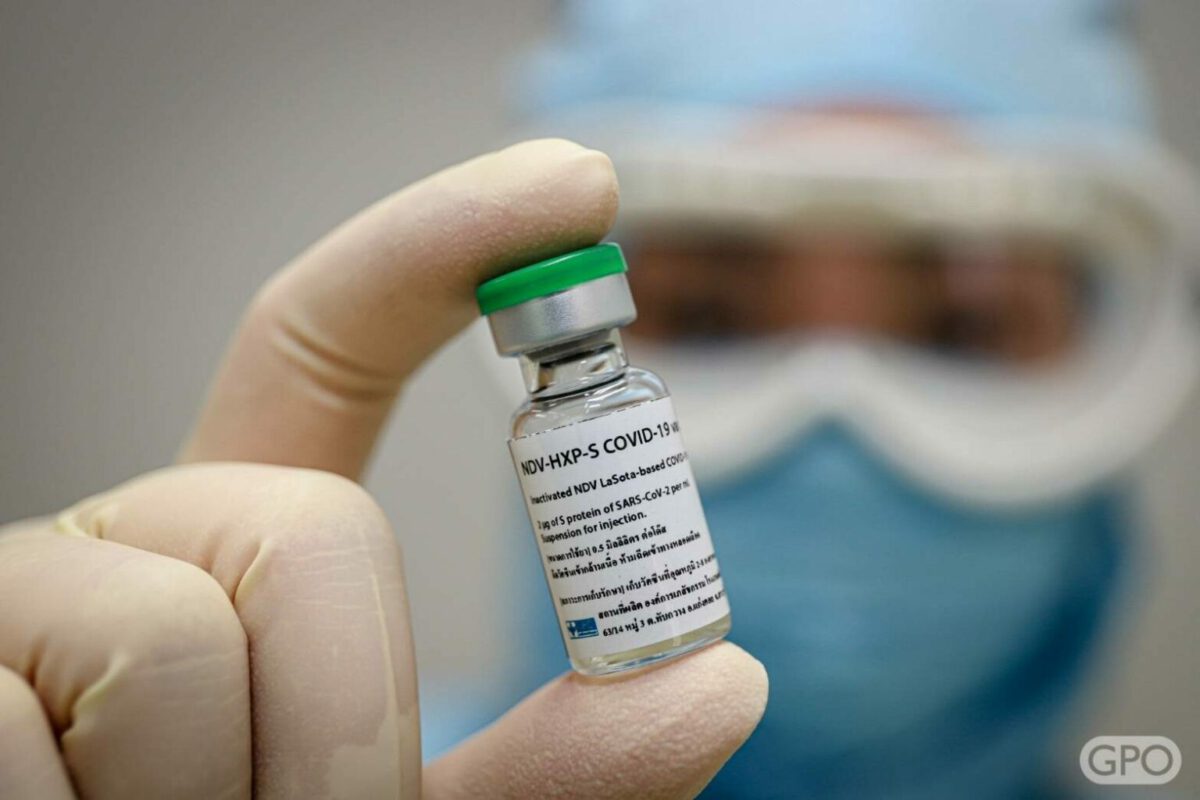
วัคซีน HXP-GPOVac เป็นวัคซีนที่คณะเวชศาสตร์เขตร้อน มหาวิทยาลัยมหิดล ร่วมกับองค์การเภสัชกรรม ศึกษาวิจัยวัคซีนป้องกันโควิด-19 ชนิดเชื้อตาย ด้วยเทคโนโลยีไข่ไก่ฟัก ที่ใช้ในการผลิตวัคซีนไข้หวัดใหญ่อยู่แล้ว และนำมาปรับใช้ในการผลิตวัคซีนโควิด-19 ซึ่งผลการทดสอบในสัตว์พบว่า มีความปลอดภัยและกระตุ้นภูมิคุ้มกันได้ดี
สำหรับการทดลองในมนุษย์ สำนักข่าวไทยพีบีเอส รายงานในวันที่ 30 มิถุนายน 2564 ว่าวัคซีนตัวดังกล่าวได้เริ่มทดลองในอาสาสมัครระยะที่ 1 เมื่อเดือนมีนาคม 2564 โดย ศ.พญ.พรรณี ปิติสุทธิธรรม รักษาการหัวหน้าศูนย์วัคซีน หัวหน้าภาควิชาอายุรศาสตร์เขตร้อน คณะเวชศาสตร์เขตร้อน มหาวิทยาลัยมหิดล กล่าวไว้ว่า ในระยะที่ 1 ได้ทำการศึกษาในอาสาสมัครที่มีสุขภาพแข็งแรง ไม่มีการติดเชื้อตับอักเสบบีและซี และไม่เป็นภูมิคุ้มกันบกพร่อง จำนวน 210 คน โดยแบ่งเป็น 6 กลุ่ม คือ กลุ่มที่ได้วัคซีนจริงในสูตรต่างๆ กัน ตั้งแต่ขนาดต่ำจนถึงขนาดสูง ทั้งที่มีและไม่มีสารเสริมฤทธิ์ เปรียบเทียบกับกลุ่มที่ได้รับสารเลียนแบบวัคซีน
ผลตรวจเบื้องต้นจากห้องปฏิบัติการทั้งในประเทศและต่างประเทศพบว่า มีภูมิคุ้มกันตอบสนองได้ดี โดยจะมีการรายงานผลการทดสอบอย่างเป็นทางการในเดือน กรกฎาคมนี้
หลังจากนี้ทีมผู้วิจัยจะทำการเลือกวัคซีน 2 ใน 5 สูตรที่ให้ผลดีที่สุด เพื่อทดลองในอาสาสมัคร 250 คน ในระยะที่ 2 ในช่วงเดือนสิงหาคม เพื่อคัดเลือกสูตรที่ดีที่สุดไปทดลองระยะที่ 3 ในภาคสนามกับอาสาสมัคร 1,000-10,000 คน โดยวัคซีนที่ผ่านการวิจัยในมนุษย์ทั้ง 3 ระยะ จะถูกนำไปขึ้นทะเบียนกับสำนักงานคณะกรรมการอาหารและยา ก่อนจะเริ่มการผลิตต่อไปเพื่อทำให้คนไทยเข้าถึงวัคซีนได้ง่ายขึ้นในราคาที่ถูกลง
ทางด้าน นพ.วิฑูรย์ ด่านวิบูลย์ ผู้อำนวยการองค์การเภสัชกรรม (อภ.) กล่าวว่า ปัจจุบันวัคซีนป้องกันโควิด-19 ทุกชนิดตั้งต้นพัฒนามาจากเชื้อไวรัสโคโรนา 2019 สายพันธุ์อู่ฮั่น ซึ่งวัคซีน HXP-GPOVac ก็เป็นการทดลองกับเชื้อไวรัสสายพันธุ์อู่ฮั่นเช่นกัน แต่ใช้เทคโนโลยีล็อคโปรตีนไวรัส 6 ตำแหน่ง ซึ่งหากเทียบกับวัคซีนตัวอื่นจะมีการล็อคโปรตีนไวรัสไว้เพียง 2 ตำแหน่งเท่านั้น ซึ่งการล็อคตำแหน่งโปรตีนหลายจุดนี้ จะทำให้ร่างกายจดจำเชื้อได้หลากหลายกว่า สร้างภูมิคุ้มกันได้กว้างกว่า เมื่อนำมาทดสอบกับสายพันธุ์อัลฟา (อังกฤษ) ก็ให้ผลลัพธ์ค่อนข้างดี ภูมิคุ้มกันไม่ได้ลดลงมากนัก
ส่วนสายพันธุ์เบตา (แอฟริกาใต้) และสายพันธุ์เดลตา (อินเดีย) อยู่ระหว่างการทดสอบในขณะนี้ที่กรมวิทยาศาสตร์การแพทย์ เพื่อดูว่าวัคซีนตอบสนองกับสายพันธุ์ใดบ้าง
อย่างไรก็ตาม สำหรับเทคโนโลยีนี้ ในรุ่นต่อไปจะมีการเปลี่ยนหัวเชื้อ หรือเปลี่ยนเชื้อต้นแบบ ซึ่งอาจจะมีการนำเชื้อหลายสายพันธุ์มารวมกัน เอา Spike Protein ของแต่ละสายพันธุ์รวมกัน เพื่อดูประสิทธิภาพของวัคซีน
จากการรายงานของสำนักข่าวไทยพีบีเอส ระบุว่า วันที่ 30 มิถุนายน ที่ผ่านมา เพจ Mahidol Channel เปิดเผยความคืบหน้าการศึกษาวิจัยวัคซีน HXP-GPOVac โดยองค์กรด้านสุขภาพระดับสากล (Program for Appropriate Technology in Health: PATH) ได้ส่งหัวเชื้อไวรัสตั้งต้นที่พัฒนาโดยโรงเรียนแพทย์ที่ Mount Sinai ในนิวยอร์ค และมหาวิทยาลัยเท็กซัสมาให้องค์การเภสัชกรรม โดยหัวเชื้อไวรัสดังกล่าวเกิดจากการตัดแต่งพันธุกรรมไวรัสนิวคาสเซิล ให้มีโปรตีนส่วนหนาม (Spike Protein) ของไวรัสโคโรนาสายพันธุ์ใหม่ 2019 อยู่ที่ผิว ซึ่งไวรัสที่ตัดแต่งพันธุกรรมนี้ไม่ก่อให้เกิดโรคโควิด-19 และสามารถเพิ่มจำนวนได้ในไข่ไก่ฟักเหมือนกันกับไวรัสไข้หวัดใหญ่ จึงทำให้มีศักยภาพในการรับไวรัสตั้งต้นดังกล่าวมาผลิตในระดับอุตสาหกรรมต่อได้
ทั้งนี้ คาดว่าภายในปี 2565 จะขอขึ้นทะเบียนตำรับยา และทำการผลิตในระดับอุตสาหกรรมที่โรงงานผลิต (วัคซีน) ชีววัตถุ ขององค์การเภสัชกรรมที่จังหวัดสระบุรี ที่ผลิตวัคซีนไข้หวัดใหญ่ ปรับมาผลิตวัคซีนโควิดแทน โดยตั้งเป้าผลิตให้ได้ 25-30 ล้านโดสต่อปี
โควิเจน
วัคซีน ‘โควิเจน’ (COVIGEN) เป็นวัคซีนชนิดดีเอ็นเอ จากบริษัท ไบโอเน็ท-เอเชีย จำกัด บริษัท ร่วมทุนไทย-ฝรั่งเศส และ บริษัท เทคโนวาเลีย (Technovalia)
ผลการทดสอบในหนูทดลองพบว่า วัคซีนมีความปลอดภัย และสร้างภูมิคุ้มกันได้ดีมาก ขณะนี้อยู่ระหว่างการยื่นขออนุมัติกับสำนักงานคณะกรรมการอาหารและยา (อย.) เพื่อทดสอบในมนุษย์ในระยะที่ 1 โดยจะมีการทดสอบทั้งไทยและออสเตรเลีย ซึ่งขณะนี้ในออสเตรเลียมีอาสาสมัครที่มีสุขภาพดีจำนวน 150 คน และผลจากการทดลองนี้จะทำให้สามารถประเมินวัคซีนสำหรับการทดลองในระยะที่ 2 และ 3 ในลำดับต่อไป
อ้างอิง
- www.redcross.or.th
- www.isranews.org
- www.biotechthailand.com
- www.hfocus.org
- news.thaipbs.or.th
- www.bbc.com
- www.pptvhd36.com
- www.bangkokbiznews.com
- www.matichon.co.th
- news.thaipbs.or.th
- workpointtoday.com
- www.linkedin.com