จากการพัฒนาวัคซีนชนิด mRNA สัญชาติไทยของศูนย์วิจัยวัคซีน คณะแพทยศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย ภายใต้ชื่อ ChulaCOV19 ขณะนี้อยู่ในช่วงการทดสอบกับมนุษย์ โดยทดสอบกับอาสาสมัครในวัย 18-55 ปี ครบทั้งสองเข็มแล้ว และอาสาสมัครวัย 56-75 ปี ส่วนใหญ่ได้ฉีดเข็มแรกแล้วและอยู่ระหว่างการรอฉีดเข็มที่สอง
วันที่ 16 สิงหาคม 2564 ศ.นพ.เกียรติ รักษ์รุ่งธรรม ผู้อำนวยการโครงการพัฒนาวัคซีนโควิด-19 ได้แถลงผลงานเบื้องต้นของการทดลองวัคซีนในระยะที่ 1 ผ่านการถ่ายทอดสดบนเฟซบุ๊คแฟนเพจโรงพยาบาลจุฬาลงกรณ์ สภากาชาดไทย โดยกล่าวว่า วัคซีนดังกล่าวได้เริ่มฉีดเข็มแรกในวันที่ 14 มิถุนายน 2564 กับอาสาสมัครกลุ่มแรกจำนวน 36 คน และขณะนี้ทั้งหมดได้รับการฉีดครบทั้งสองเข็มแล้ว อย่างไรก็ตาม ผลการรายงานครั้งนี้คือผลช่วง 7 วัน หลังจากการรับวัคซีนเข็มสองของอาสาสมัครกลุ่มแรก ส่วนอาสาสมัครกลุ่มที่สองที่มีอายุ 56-75 ปี อีก 36 คน ส่วนใหญ่ได้ฉีดเข็มแรกแล้ว และกำลังรอฉีดเข็มที่สองต่อไป
ศ.นพ.เกียรติ คาดว่าก่อนสิ้นเดือนนี้จะเริ่มทดลองเฟส 2a ในจำนวนอาสาสมัคร 150 คน โดย 120 คน จะได้รับวัคซีน ChulaCOV19 ซึ่งเลือกจากขนาดที่เหมาะสมจากระยะที่ 1 และอีก 30 คน จะได้รับวัคซีน Pfizer แทนการฉีดวัคซีนหลอก เนื่องจากขณะนี้ไทยได้รับ Pfizer เข้ามาแล้ว เพื่อทำการเปรียบเทียบในเชิงวิชาการ
ส่วนเรื่องความปลอดภัยและปฏิกิริยาผลข้างเคียงจากวัคซีน พบว่า ในอาสาสมัคร 36 คน ยังไม่ได้มีผลข้างเคียงใดๆ ที่รุนแรง ส่วนใหญ่มีอาการในระดับน้อยถึงปานกลางเท่านั้น เช่น เจ็บบริเวณที่ฉีดเช่นเดียวกับการฉีดวัคซีนทั่วไป และมีอาการอ่อนเพลีย มีไข้ ปวดกล้ามเนื้อ ซึ่งส่วนใหญ่พบในผู้ที่ฉีดเข็มที่สอง
ทั้งนี้ ศ.นพ.เกียรติ สรุปผลเบื้องต้นของวัคซีน ChulaCov19 ในเฟสที่ 1 ดังนี้
1. วัคซีน ChulaCov19 สามารถกระตุ้นภูมิคุ้มกันชนิด antibody ได้สูงเทียบเท่าวัคซีนชนิด mRNA ตัวอื่น เช่น Pfizer โดยจากการทดลองพบว่า ผลภูมิคุ้มกันในกลุ่มอาสาสมัครสามารถยับยั้งการจับของ RBD (receptor-binding domain) หรือโปรตีนส่วนปุ่มหนาม ซึ่งหากแย่งจับได้ จะทำให้ไวรัสไม่สามารถเข้าเซลล์ได้ และผลออกมาว่า ChulaCOV19 มีความสามารถยับยั้งสูงเท่า Pfizer ที่ 94 เปอร์เซ็นต์ วัคซีน AstraZeneca 84 เปอร์เซ็นต์ และ Sinovac 75 เปอร์เซ็นต์ ซึ่งหากมีตัวเลขเกิน 70 เปอร์เซ็นต์ จะถือว่ามีประสิทธิภาพในการป้องกันการติดเชื้อไวรัสได้
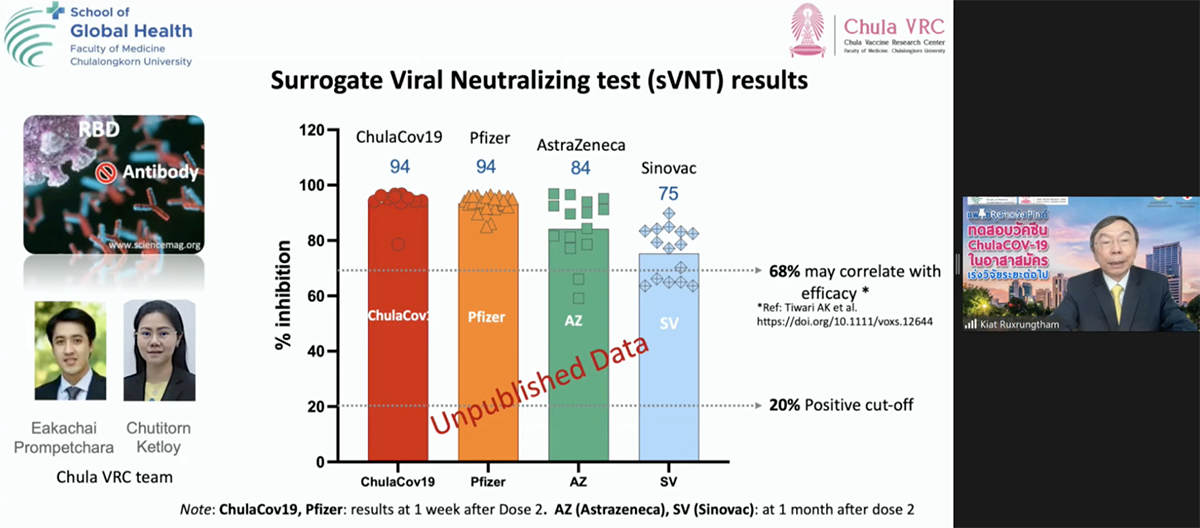
อีกทั้งเมื่อตรวจเชื้อไวรัสที่ได้ทำการเพาะเลี้ยงแต่ละสายพันธุ์เพื่อดูว่าภูมิคุ้มกันในเลือด หรือ antibody สามารถยับยั้งไม่ให้ไวรัสเข้าเซลล์ในหลอดทดลองที่ทำการศึกษาได้หรือไม่ ผลพบว่าเมื่อเทียบเข็มที่ 1 และ 2 ระหว่าง ChulaCOV19 กับ Pfizer พบว่า 3 อาทิตย์หลังฉีดเข็ม 1 และ 2 มีภูมิขึ้นสูงใกล้เคียงกัน
2. กระตุ้น antibody ได้สูง ในการยับยั้งเชื้อสายพันธุ์ดั้งเดิม
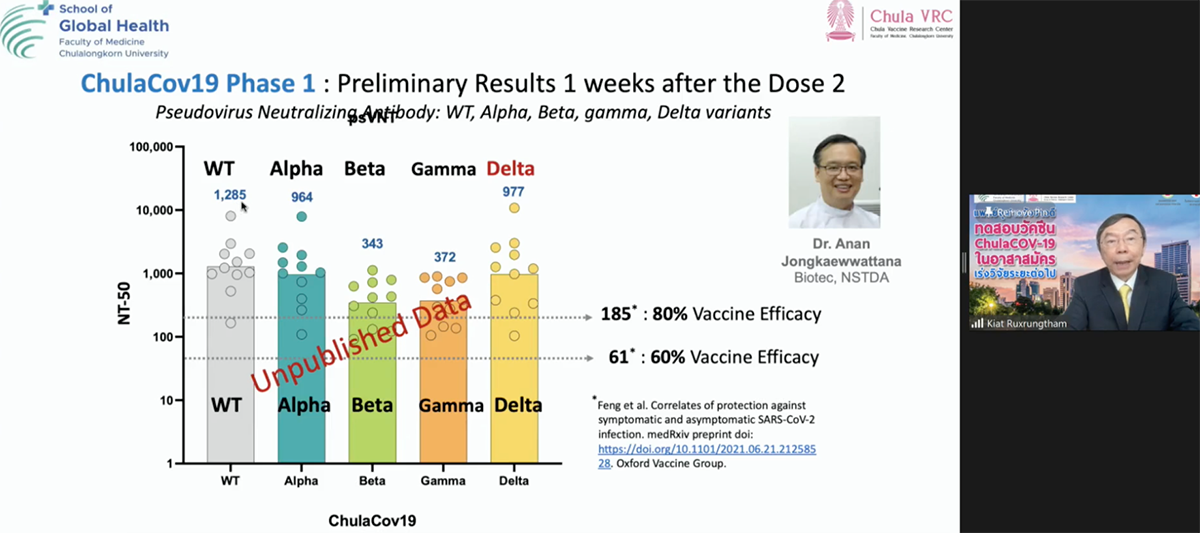
3. antibody ที่สูง สามารถยับยั้งเชื้อข้ามสายพันธุ์ได้ทั้ง 4 สายพันธุ์ คือ อัลฟา เบตา แกมมา และ เดลตา
จากการทดลองในแล็บของ ดร.อนันต์ จงแก้ววัฒนา นักไวรัสวิทยา ผู้อำนวยการกลุ่มวิจัยนวัตกรรมสุขภาพสัตว์และการจัดการ ศูนย์พันธุวิศวกรรมและเทคโนโลยีชีวภาพแห่งชาติ (ไบโอเทค) สำนักงานพัฒนาวิทยาศาสตร์และเทคโนโลยีแห่งชาติ (สวทช.) ซึ่งได้ทำการทดลองด้วยเทคนิค Pseudovirus Neutralization Assay หรือการตรวจปริมาณ antibody ชนิด NAb ที่สามารถยับยั้งการเข้าสู่เซลล์ของไวรัส พบว่า วัคซีน ChulaCOV19 อยู่ในเกณฑ์ที่ดีในการยับยั้งเชื้อทั้งสายพันธุ์ดั้งเดิมและสายพันธุ์ใหม่
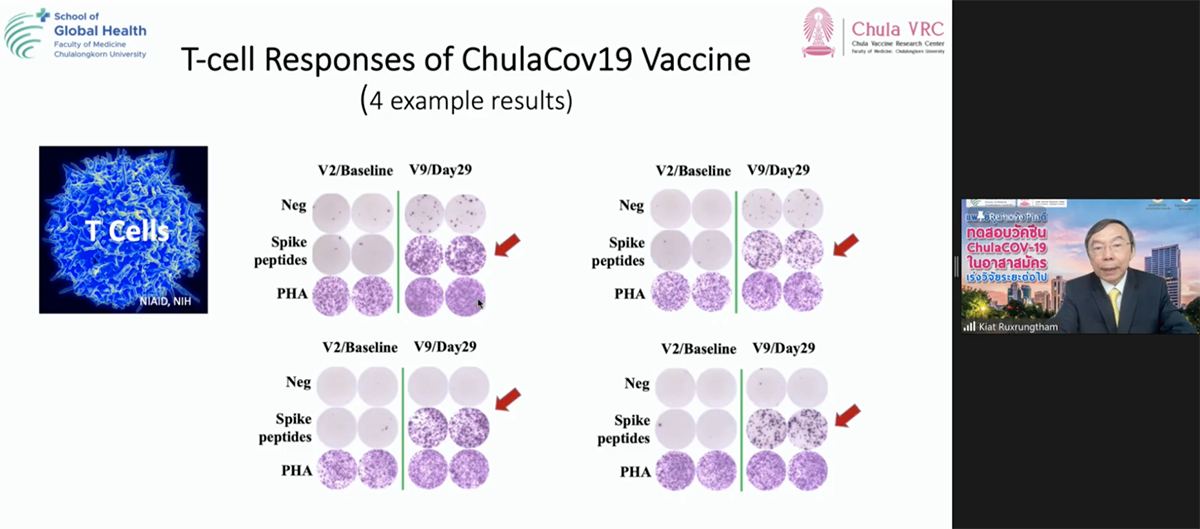
4. สามารถกระตุ้นภูมิคุ้มกันชนิด T-cell ซึ่งจะช่วยขจัดและควบคุมเชื้อที่อยู่ในเซลล์ของคนที่ติดเชื้อได้ โดย ศ.นพ.เกียรติ กล่าวว่า ภูมิคุ้มกันที่สำคัญนอกจากในน้ำเหลืองที่ป้องกันไม่ให้เชื้อเข้าเซลล์ เมื่อเชื้อเข้าเซลล์แล้วต้องมีภูมิระดับเซลล์ที่ไปขจัดภูมิเนื้อเยื่อหรือเซลล์ที่มีเชื้อ SARS-CoV-2 หรือติดเชื้อไวรัสโควิด-19 ที่ทำให้เกิดโรคโควิด-19 พบว่าหลังฉีดวัคซีน ChulaCOV19 เข็มสองได้ 7 วัน จำนวนเซลล์ที่ถูกกระตุ้นมีมากขึ้น จึงถือได้ว่าอาสาสมัครที่ได้รับวัคซีนมีภูมิสูงขึ้น
อย่างไรก็ตาม ศ.นพ.เกียรติ ย้ำว่าข้อมูลทั้งหมดนี้ยังไม่ได้มีการตีพิมพ์อย่างเป็นทางการ
นอกจากนี้ ในขั้นตอนการขึ้นทะเบียน ขณะนี้วัคซีน ChulaCOV19 ได้ผ่านเฟส 1 มาแล้ว และปลายสัปดาห์นี้จะมีการประชุมเพื่อเลือกโดสที่ปลอดภัยและป้องกันไวรัสที่ข้ามสายพันธุ์ได้ไปทดลองต่อไป โดยคาดว่าปีหน้าคนไทยน่าจะได้รับวัคซีนเกิน 70-80 เปอร์เซ็นต์ ดังนั้น วัคซีนที่จะขึ้นทะเบียนจะต้องมีข้อมูลเพียงพอที่จะเป็นวัคซีนกระตุ้นเข็มสาม จึงได้ทำการเตรียมงบและหาทุนต่อไป
ส่วนโรงงานที่ผลิต ศ.นพ.เกียรติ ให้ข้อมูลว่าได้บริษัท BioNet-Asia ที่มีโรงงานอยู่ที่จังหวัดพระนครศรีอยุธยา โดยพร้อมถ่ายทอดเทคโนโลยี mRNA ให้ทางฝ่ายผลิตได้ผลิตต่อไป และคาดว่าเดือนตุลาคมน่าจะมีวัคซีนที่ผลิตโดยคนไทย 100 เปอร์เซ็นต์
อย่างไรก็ตาม หากประเทศไทยต้องการได้วัคซีนโดยเร็วที่สุด ศ.นพ.เกียรติ กล่าวว่า ภายในเมษายน 2565 สามารถทำได้ แต่ต้องมีองค์ประกอบ 4 อย่าง คือ
- ประเทศไทยต้องไม่บริหารทุนแบบเดิม คือ ต้องมีเป้าหมายร่วมกันทั้งภาครัฐ เอกชน และประชาชน เพราะมีงบเพียงพอ รวดเร็ว และมีประสิทธิภาพในการตัดสินใจได้
- กติกาการขึ้นทะเบียนวัคซีนของ อย. ต้องมีความชัดเจน เช่น จะทำถึงระดับ 2b หรือระยะ 3 อย่างไรจึงจะเพียงพอ และต้องชนะหรือดีเท่าวัคซีนที่ขึ้นทะเบียนในประเทศไทยหรือไม่
- โรงงานไทยต้องเร่งดำเนินการผลิตวัคซีนให้มีคุณภาพและมีจำนวนมากได้ก่อนสิ้นปีนี้
- นโยบายการจองวัคซีนล่วงหน้าของรัฐหรือแม้แต่ภาคเอกชนเอง จะต้องมีความชัดเจน